第五单元 化学方程式 课题1 水平守恒定律(测试)
(时间:45分钟 满分:100分)
学校:___________ 名字:__________ 班级:__________ 得分:
1、单选题(13个小题,每小题5分,共65分)
1.下列化学符号中,既能表示一个原子,又能表示一种元素,还能表示一种物质的是
A.H2 B.O C.He D.CO
【答案】C
【分析】
依据元素符号的意思进行剖析解答。金属、固体非金属、稀少气体都是由原子直接构成的,故它们的元素符号,既能表示一个原子,又能表示一种元素,还能表示一种物质。
元素符号能表示一种元素,还能表示该元素的一个原子;化学式能表示一种物质;当元素符号又是化学式时,就同时拥有了上述三层意义。A、该符号是氢气的化学式,表示氢气这种物质和一个氢气分子,不可以表示一种元素,故A错误;B、O是可表示氧元素,表示一个氧原子,但不可以表示一种物质,故B错误;C、He是稀少气体元素,可表示氦元素,表示一个氦原子,还能表示氦气这一物质,故C正确;D、该符号是一氧化碳的化学式,不是元素符号,故D错误。故选C。
2.工业上用甲和乙反应制备燃料丙.依据微观示意图得出的结论中,正确的是()

A.丙中碳和氢元素的水平比为1:3 B.汽油中加入丙,不可以降低汽车尾气污染
C.甲、乙、丙都是有机物 D.反应中甲、乙、丙的分子个数比为1:1:1
【答案】D
【分析】A、依据丙的化学式是C2H6O可知该物质中碳氢两种元素的水平比为:2×12:1×6=4:1;B、汽油中加入C2H6O,因为它能燃烧,且产物是水与二氧化碳,所以可有效地减少汽油的消耗,从而减小了对空气的污染;C、有机物是含碳的化合物,所以甲丙均是有机物,而乙是水不含碳所以不是有机物;D、该反应的方程式C2H4+H2O=C2H6O可知反应中甲、乙、丙的分子个数比为1:1:1;故选D。
3.“珍惜生命,拒绝毒品”,特别是青少年更应该对毒品说不,如吸食“冰毒”,易成瘾,有害地方强,会紧急破坏人体的生理和免疫功能,冰毒的主要成分是甲基苯丙胺(C10H15 N)。下列说法正确的是
A.甲基苯丙胺含26个原子
B.甲基苯丙胺的相对分子水平为149 g
C.甲基苯丙胺由碳、氢、氮三种元素组成
D.甲基苯丙胺中各元素的水平比为10:15:1
【答案】C
【分析】
A、甲基苯丙胺是由分子构成的,由化学式可知,一个甲基苯丙胺分子含 26 个原子,故A错误;B、相对分子水平的单位符号是“1”,不是“g”,甲基苯丙胺的相对分子水平为149,故B错误;C、甲基苯丙胺由碳、氢、氮三种元素组成,故C正确;D、化学式中元素符号右下角的数字为一个分子中原子的个数,甲基苯丙胺中各元素的原子个数比为10:15:1,水平比为(12×10):(1×15):(14×1)=120:15:14,故D错误。故选C。
4.如图形象地表示某化学反应前后反应物与生成物分子及其数目的变化,![]() 、
、![]() 、
、![]() 分别表示A、B、C三种不同物质的分子。该反应的化学方程式中A、B、C前的化学计量数之比为
分别表示A、B、C三种不同物质的分子。该反应的化学方程式中A、B、C前的化学计量数之比为
A.1∶4∶3 B.1∶![]() 3∶2 C.3∶1∶2 D.3∶1∶3
3∶2 C.3∶1∶2 D.3∶1∶3
【答案】C
【分析】依据反应的微观示意图和水平守恒定律,可得出各物质反应的微粒个数关系是:
由上图可知,反应前有1个A分子而反应后没A分子,说明1个A分子参加反应;反应前有3个B分子而反应后没B分子,说明3个3分子参加反应;反应前没C分子,反应后生成了2个C分子.所以,该反应中A、B、C各物质的微粒个数关系是:1:3:2.因此,该反应的化学方程式中A、B、C前的化学计量数之比为1:3:2。学科~网
5.将肯定水平的a,b,c,d四种物质放入一密闭容器中,在肯定条件下反应一段时间后,测得各物质的水平如表:
物质 | a | b | c | d |
反应前的水平/g | 6.4 | 14.0 | 3.2 | 1.0 |
反应一段时间后的水平/g | 10.0 | 7.2 | x | 1.0 |
下列有关说法正确的是
A.a和b是反应物 B.x=3.2 C.d肯定是催化剂 D.该反应是分解反应
【答案】D
【分析】由题中信息知,A.b是反应物,a是生成物。故A错误。B.x=6.4.故B错误。C.d可能不是催化剂。故C错误。D.该反应是分解反应。故D正确。
6.气体烙体是一种以气体X为燃料的加热仪器,加热温度可达1300℃反应的化学方程式为2X+13O2______________________________8CO2+10H2O,燃料X的化学式( )
A.C4H10 B.C3H8 C.C2H5OH D.CH3OH
【答案】A
【分析】由水平守恒定律:反应前后,原子类型、数目均不变,据此由反应的化学方程式判断反应物X的化学式。解:由水平守恒定律:反![]() 应前后,原子类型、数目均不变,由反应的化学方程式2X+13O2____________________8CO2+10H2O,反应前氧原子个数为26,反应后的生成物中碳、氢、氧原子个数分别为8、20、26、依据反应前后原子类型、数目不变,则2X分子中含有8个碳原子和20个氢原子,则每一个X分子由4个碳原子和10个氢原子构成,则物质X的化学式为C4H10。故选:A。
应前后,原子类型、数目均不变,由反应的化学方程式2X+13O2____________________8CO2+10H2O,反应前氧原子个数为26,反应后的生成物中碳、氢、氧原子个数分别为8、20、26、依据反应前后原子类型、数目不变,则2X分子中含有8个碳原子和20个氢原子,则每一个X分子由4个碳原子和10个氢原子构成,则物质X的化学式为C4H10。故选:A。
7.下列变化,遵循水平守恒定律的是
A.石墨制成金刚石 B.2gH2完全燃烧生成36gH2O
C.水变成汽油 D.冰转化成干冰
【答案】A
【分析】水平守恒定律是参加反应的各物质的水平总和等于反应后生成的各物质的水平总和。即水平守恒定律研究化学变化的 水平问题。由水平守恒定律可知反应前后元素类型不变。A石墨制成金刚石,是化学变化,遵循水平守恒定律;B.2gH2完全燃烧生成18gH2O;C.水中无氢元素,不可能变成汽油; D.冰是固态的水,干冰是固态二氧化碳,组成元素不同,不可以相互转化。选A
8.已知分别表示X、Y、Z三种不一样的气体分子,在肯定条件下的变化如图所示,由图示获得的下列信![]() 息中正确的是
息中正确的是
A.反应后有气体单质生成 B.反应前后分子、原子类型均不变
C.反应后容器内的物质为![]() 纯净物 D.该反应可表示为3X + Y = 2Z
纯净物 D.该反应可表示为3X + Y = 2Z
【答案】D
【分析】A.由一种元素组成的纯净物叫单质;由不同元素组成的纯净物叫化合物;B.反应前后分子类型改变,原子的类型没改变;原子是化学变化中最小的微粒。C.反应后容器内有两种物质为混合物;D.由图可知,该反应可表示为3X + Y = 2Z;选D 学科¥网
9.在“宏观﹣﹣微观﹣﹣符号”之间打造联系是化学学科特有些思维方法.如图是某化学反应的微观模拟示意图![]() ,依据该图判断下列说法中
,依据该图判断下列说法中![]() 正确的是
正确的是
A.图中的反应物都是单质 B.该反应的化学方程式是 H2O+C![]() CO+H2
CO+H2
C.化学反应前后碳元素化合价没改变 D.该反应是分解反应
【答案】B
【分析】A、反应物一氧化碳是不同种元素组成的化合物,故错误;B、该反应为水在高温条件下与单质碳反应生成一氧化碳和氢气,反应的化学方程式为H2O+C![]() CO+H2,故正确;C、反应前单质碳中碳元素为0价,而反应后一氧化碳中碳元素为+2价,化学反应前后碳元素化合价发生改变,故错误;D、反应为单质碳与化合物水生成化合物一氧化碳和单质氢气,是置换反应,故错误。
CO+H2,故正确;C、反应前单质碳中碳元素为0价,而反应后一氧化碳中碳元素为+2价,化学反应前后碳元素化合价发生改变,故错误;D、反应为单质碳与化合物水生成化合物一氧化碳和单质氢气,是置换反应,故错误。
10.在化学反应A+2B=C+2D中,m克A物质与n克B物质恰好完全反应生成e克C物质,则同时生成的D物质水平为
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
【答案】D
【分析】依据水平守恒定律知,生成的D物质水平为![]() 。
。
11.如图为汽车尾气净化装置中发生反应的微观示意图。有关叙述错误的是()

A.图中单质的化学式为N2 B.该反应是化合反应
C.反应后分子总数降低 D.该装置可净化汽车尾气
【答案】B
【分析】该反应的反应物是NO和CO,生成物是CO2和N2,该反应的化学方程式为:2NO+2CO ![]() 2CO2+N2;A、由上述剖析可知,图中单质的化学式为N2,故正确;B、由上述反应可知,该反应的生成物是两种物质
2CO2+N2;A、由上述剖析可知,图中单质的化学式为N2,故正确;B、由上述反应可知,该反应的生成物是两种物质![]() ,不是化合反应,故错误;C、由上述反应可知,每4个分子反应生成了3个分子,故分子总数降低,故
,不是化合反应,故错误;C、由上述反应可知,每4个分子反应生成了3个分子,故分子总数降低,故![]() 正确;D、该装置能将汽车尾气中的一氧化碳和一氧化氮转化为无毒的二氧化碳和氮气,故正确。
正确;D、该装置能将汽车尾气中的一氧化碳和一氧化氮转化为无毒的二氧化碳和氮气,故正确。
12.甲和乙可以合成清洗燃料丙,微观过程如图。下列说法错误的是

A.丁的化学式为H2O B.丙中C、H、O的水平比为12:3:8
C.该反应中有三种氧化物 D.参加反应的甲和乙的水平比是7:1
【答案】C
【分析】甲物质的化学式为CO、乙物质的化学式为H2、丙物质的化学式为C2H6O,结合水平守恒定律化学反应前后原子的类型和个数都不变可知丁的化学式为H2O,因此反应的方程式为:2CO+4H2 ![]() C2H6O+H2O,因此:A、丁的化学式为H2O,故说法正确;B、丙是C2H6O,其中C、H、O的水平比为(12×2 ):(1×6):16=12:3:8,故说法正确;C、由方程式可知,该反应中有CO、H2O两种氧化物,故说法不正确;D、由方程式可知,参加反应的甲和乙的水平比是:【2×(12+16)】:【4×1×2】=7:1,故说法正确。
C2H6O+H2O,因此:A、丁的化学式为H2O,故说法正确;B、丙是C2H6O,其中C、H、O的水平比为(12×2 ):(1×6):16=12:3:8,故说法正确;C、由方程式可知,该反应中有CO、H2O两种氧化物,故说法不正确;D、由方程式可知,参加反应的甲和乙的水平比是:【2×(12+16)】:【4×1×2】=7:1,故说法正确。
13.“尾气催化转化器”可以将汽车尾气中有毒气体转变为无毒气体,下面是其中一个化学反应的微观示意图,其中不一样的圆球代表不一样的原子。从图中获得信息不正确的是
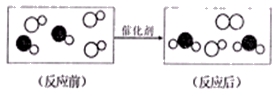
A.分子是可以运动的 B.分子间存在着肯定的空隙
C.图中生成物均为化合物 D.参加反应的两种分子的个数比为1:1
【答案】C
【分析】A.分子是可以运动的,通过运动相互接触而发生反应;B.由图可知分子间存在着一![]() 定的空隙;C.由同种分子构成的物质是纯净物,由原子直接构成物质时,一种原子构成一种物质,由不同元素组成的纯净物叫化合物。图中生成物为化合物和单质;D.由图中信息可知参加反应的两种分子的个数比为1:1。选C
定的空隙;C.由同种分子构成的物质是纯净物,由原子直接构成物质时,一种原子构成一种物质,由不同元素组成的纯净物叫化合物。图中生成物为化合物和单质;D.由图中信息可知参加反应的两种分子的个数比为1:1。选C
2、非选择题(共35分)
14. (11分)日常食盐除去可作调味品外,当玻璃杯里结了茶垢后也可以用食盐擦洗, 去污成效很好.食盐的主要成分NaCl中氯元素的化合价为_____;除去食盐水中泥沙等不溶性杂质的办法是_________;氯化钠还可用于制造纯碱,原理是向饱和食盐水中先后通入足量的NH3和CO2,生成小苏打(在该溶液中难溶)和一种氮肥,推断该氮肥的化学式_____.
【答案】﹣1 价 ;过滤 ;NH4Cl .
【分析】
依据在化合物中正负化合价代数和为零,结合氯化钠的化学式进行解答即可;过滤是把不溶于液体的固体与液体离别的一种办法;依据水平守恒定律,反应前后元素类型不变,进行剖析解答。
钠元素显+1价,设氯元素的化合价是x,依据在化合物中正负化合价代数和为零,可得:(+1)+x=0,则x=-1价;过滤是把不溶于液体的固体与液体离别的一种办法,除去食盐水中泥沙等不溶性杂质可使用过滤的办法;氯化钠还可用于制造纯碱,原理是向饱和食盐水中先后通入足量的NH3和CO2,生成小苏打(在该溶液中难溶)和一种氮肥,由反应前后元素类型不变,该氮肥为氯化铵,其化学式为:NH4Cl。
15. (12分)下图是某化学变化的微观示意图,X、Y、Z分别表示不相同种类别的原子,据图回答问题:
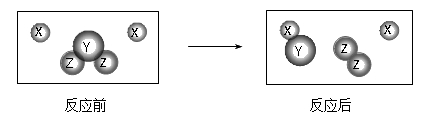
(1)该化学反应中生成物的分子个数比为_____;
(2)由X原子构成的物质在该反应中_____(填“是”或“不是”)催化剂;
(3)从微观角度剖析,化学反应前后各物质的水平总和相等![]() 是什么原因___________。
是什么原因___________。
【答案】 1:1 不是 化学反应前后原子的类型、数目和水平都不变
【分析】在示意图中,其中的X原子没完全参加反应,因此反应的方程式为:X+YZ2=XY+Z2,则:(1)依据方程式可知该化学反应中生成物的分子个数比为1:1;(2)由微粒的变化可知,X是反应物,只不过没完全参加反应,因此不是催化剂;(3)由微粒的变化可知,化学反应前后原子的类型、数目和水平都没发生改变,因此化学反应前后各物质的水平总和相等。
16.(12分)下图是某反应前后分子变化的微观示意图:
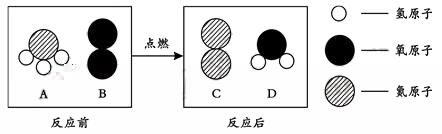
请回答以下问题:
(1)四种物质中,是化合物的有________(填图中字母)。
(2)该反应中,没发生变化的微粒是_______(用微粒符号表示)。
(3)在该反应中,参加反应的A和B的水平比为______(计算结果用最简整数比表示)。
【答案】 AD ; H、O、N; 17:24
【分析】








